Terapia mRNA sintetica: studio introduce arma contro cancro metastatico senza effetti collaterali dannosi
Le metastasi del cancro, ovvero la diffusione del cancro agli organi, sono una delle principali cause di morte correlate al cancro. Una volta che il cancro si diffonde a più organi, i trattamenti convenzionali come chirurgia, radioterapia e chemioterapia diventano meno efficaci. Gli scienziati della Shinshu University School of Medicine hanno sviluppato un mRNA sintetico che, quando iniettato, rivitalizza il sistema immunitario per riconoscere e attaccare le cellule tumorali metastatiche. Questa svolta potrebbe portare a nuove terapie per migliorare i tassi di sopravvivenza dei pazienti oncologici.
Il cancro continua a rappresentare una sfida importante per la salute globale, con preoccupanti tendenze di aumento dei casi. Le metastasi, ovvero la diffusione delle cellule tumorali dai tumori primari agli organi distanti, rappresentano il più grande ostacolo al successo del trattamento e sono responsabili della maggior parte dei decessi correlati al cancro. Questo processo è intricato e coinvolge cellule tumorali, componenti immunitarie e tessuti circostanti.
Le cellule tumorali usano strategie sofisticate per sopprimere il sistema immunitario e diffondersi nel corpo. Ad esempio, le cellule immunitarie come le cellule natural killer (NK) e i linfociti T citotossici (CTL), responsabili dell’attacco ai tumori, vengono riprogrammate per creare un ambiente immunosoppressivo, rendendo più difficile per il corpo reagire. Inoltre, queste cellule spesso diventano disfunzionali o esaurite, perdendo la loro capacità di uccidere efficacemente le cellule tumorali.
Il team di ricerca, guidato dal professor Sachie Hiratsuka e dal professore associato Takeshi Tomita della Shinshu University School of Medicine, insieme al professor Yoshihito Ueno della Gifu University, ha sviluppato un RNA messaggero sintetico (s-mRNA) che attiva le cellule immunitarie per contrastare questa soppressione. L’mRNA può essere iniettato per via endovenosa nel corpo, rafforzando la risposta immunitaria contro le cellule tumorali metastatiche.
Questi risultati, pubblicati online sulla rivista Nature Communications il 25 febbraio 2025, potrebbero aprire la strada a nuove terapie antitumorali. “Questo studio introduce un metodo promettente per prevenire le metastasi tumorali. Se ulteriormente sviluppato, potrebbe migliorare i tassi di sopravvivenza al cancro”, afferma il dott. Tomita.
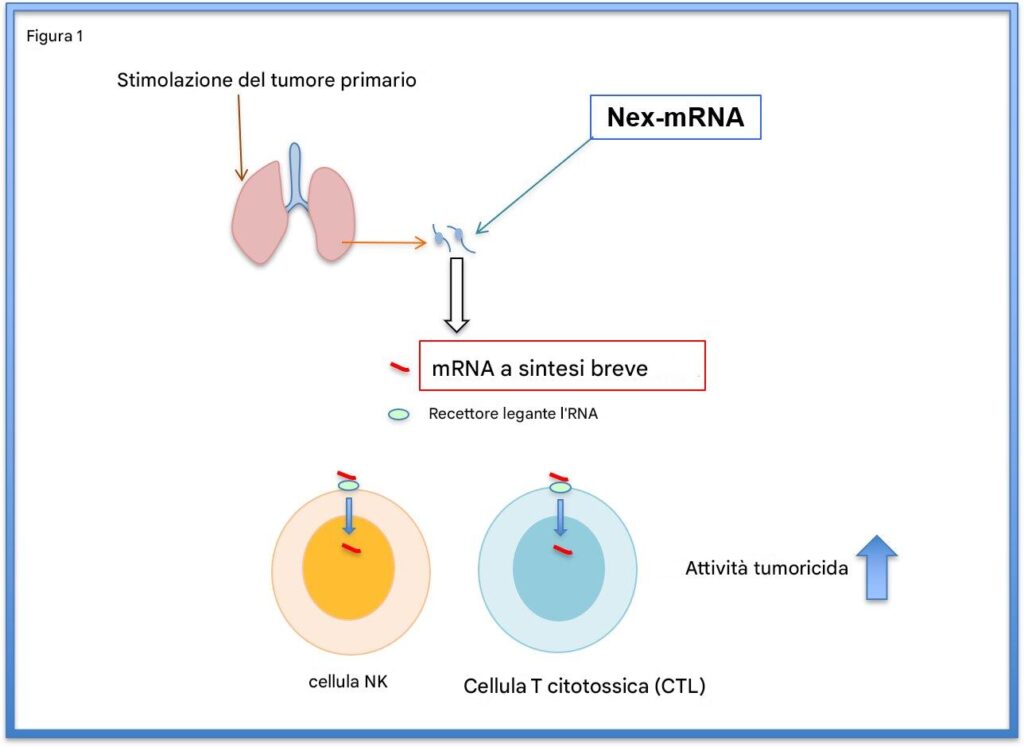
I ricercatori hanno basato il loro s-mRNA su IL1β-mRNA a lunghezza intera, che avevano originariamente identificato nei polmoni dei topi prima che si verificassero le metastasi. Questo mRNA attiva le cellule immunitarie legandosi a ZC3H12D, una proteina legante l’RNA sulle cellule NK. Tuttavia, l’IL1β-mRNA naturale è instabile e si degrada rapidamente a causa delle RNasi (enzimi che scompongono le molecole di RNA).
Per aumentare la stabilità, i ricercatori hanno progettato un IL1β-mRNA sintetico più corto, che conserva la sequenza immunostimolante essenziale che si lega al recettore ZC3H12D. Hanno anche modificato chimicamente l’mRNA per proteggerlo dalla degradazione da parte delle RNasi, consentendogli di rimanere intatto nel siero di topi e umani fino a 48 ore.
Quando iniettato per via endovenosa, l’mRNA si lega alle cellule NK e ai CTL ed entra nel nucleo, dove innesca la produzione di GZMB, una molecola chiave per l’attività di uccisione del tumore. È importante notare che questo processo non provoca una tempesta di citochine, che è una reazione eccessiva dannosa del sistema immunitario .
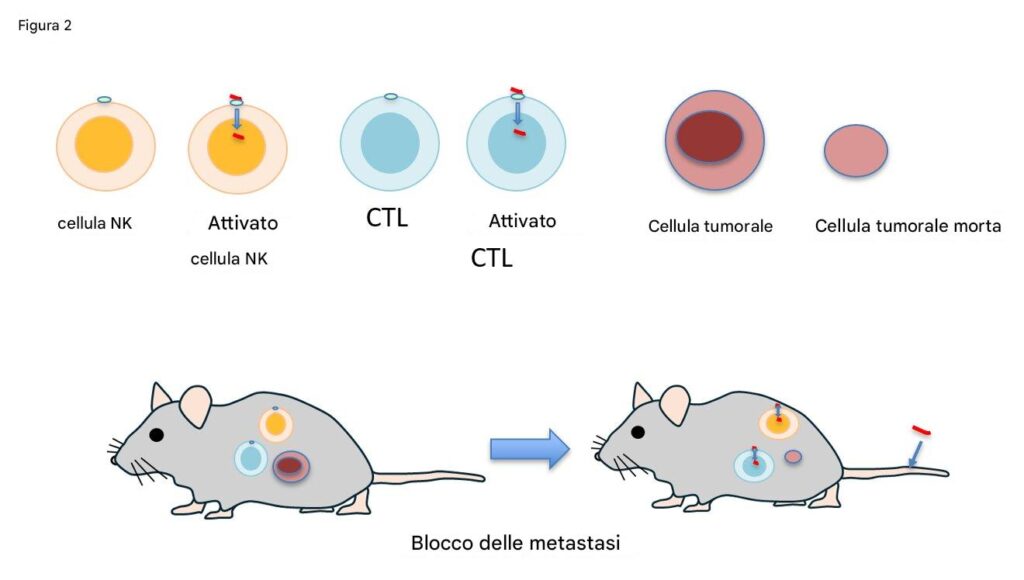
Per valutarne l’efficacia, i ricercatori hanno somministrato l’s-mRNA a topi portatori di tumore, imitando le metastasi dei tumori primari. Ai topi sono state impiantate cellule di cancro al seno (E0771) e di cancro al colon (MC-38) per creare tumori primari e le cellule tumorali sono state iniettate nel flusso sanguigno per stimolare le metastasi. Sorprendentemente, solo tre piccole dosi di s-mRNA, ciascuna di appena 1 μg, iniettate nella vena della coda del topo, hanno ridotto significativamente il numero di cellule metastatiche nei polmoni.
È importante notare che le cellule immunitarie hanno mantenuto le loro capacità di combattere il tumore per diversi giorni dopo la somministrazione di mRNA. Nei modelli di topi che simulavano metastasi dopo un intervento chirurgico, in cui il tumore primario era stato rimosso chirurgicamente, i topi che avevano ricevuto il trattamento con sIL1β-mRNA avevano significativamente meno focolai metastatici (piccoli cluster di cellule tumorali che rappresentano le fasi iniziali di metastasi) 21 giorni dopo la somministrazione rispetto al gruppo di controllo.
L’mRNA ha anche mostrato risultati promettenti per l’uso nei pazienti umani. Quando iniettato in cellule immunitarie indebolite prelevate da pazienti con cancro al colon, l’s-mRNA le ha riattivate, consentendo loro di uccidere il 70% delle cellule tumorali. Il trattamento è stato efficace anche nei pazienti sottoposti a terapia farmacologica antitumorale o in quelli con tumori multipli, superando l’IL-12, una citochina nota per stimolare le cellule immunitarie. Inoltre, il trattamento con mRNA potrebbe essere combinato con altre terapie come gli anticorpi anti-PD1 per migliorare ulteriormente i risultati.
Grazie alla sua sicurezza, facilità di somministrazione ed efficacia contro le cellule metastatiche, questo trattamento promette bene nei casi in cui le terapie tradizionali contro il cancro spesso falliscono. “Uno dei principali vantaggi del trattamento con s-mRNA è che può essere somministrato in dosi multiple senza causare effetti collaterali infiammatori indesiderati”, afferma il Prof. Hiratsuka. Questa svolta potrebbe portare a nuovi trattamenti che funzionano in modo indipendente o in combinazione con le terapie esistenti, migliorando significativamente i tassi di sopravvivenza dei pazienti con cancro metastatico.

