I cuori di maiale tenuti in vita fuori dal corpo per più di 24 ore offrono speranza a molti esseri umani che necessitano di un trapianto
Cinquantasei anni dopo il primo trapianto di cuore da uomo a uomo, ogni anno in tutto il mondo vengono trapiantati più di 5.000 cuori. Questo numero è lungi dall’essere sufficiente per dare un cuore nuovo a chiunque ne abbia bisogno, con un massimo di 50.000 persone che ne hanno bisogno in qualsiasi momento.
A seconda di quanto sono malati e di fattori fisiologici e logistici, i candidati possono aspettare anni. Un collo di bottiglia è la disponibilità di cuori di donatori idonei , in parte a causa della finestra temporale molto breve per il trapianto una volta che il cuore viene rimosso dal donatore deceduto.
L’attuale “gold standard” per preservare i cuori dei donatori è la conservazione statica a freddo (CSS), dove i cuori vengono mantenuti nel ghiaccio fino al trapianto. Il trapianto ha più successo quando la CSS dura meno di sei ore, prima che il cuore o i suoi vasi sanguigni subiscano danni.
Talvolta sono possibili periodi fino a 12 ore, ma richiedono un supporto vitale meccanico come l’ossigenazione extracorporea a membrana (ECMO) per diversi giorni sul ricevente. Prolungare il periodo di conservazione oltre le sei ore senza la necessità dell’ECMO rappresenterebbe quindi una svolta medica.
Ora, i ricercatori che hanno pubblicato su Frontiers in Cardiovascolare Medicine hanno dimostrato che è possibile mantenere in vita i cuori di maiale trapiantati fuori dal corpo per più di 24 ore utilizzando un processo chiamato perfusione cardiaca ex vivo normotermica (NEHP).
“Se trasferito agli esseri umani, questo rappresenterebbe un notevole miglioramento rispetto alla finestra temporale di sei ore nella pratica clinica standard”, ha affermato il dottor Robert Bartlett, professore emerito e capo dell’Extracorporeal Life Support Laboratory presso l’Università del Michigan Medical. Scuola ad Ann Arbor.
Continua a pompare
NEHP significa che i cuori, una volta rimossi dal donatore, vengono mantenuti in uno stato parzialmente fisiologico a temperatura ambiente pompando attraverso di essi un fluido ossigenato e ricco di sostanze nutritive (“perfusato”) derivato dal plasma sanguigno fino al trapianto. Attraverso il perfusato possono essere somministrati farmaci e cellule staminali per la riparazione dei tessuti. Attualmente, l’unica variante del NEHP approvata per uso clinico dalla Food and Drug Administration statunitense è Transmedics-OCS, che come CSS è limitata a sei ore.
Negli ultimi sette anni, l’Extracorporeal Life Support Laboratory ha lavorato per estendere costantemente la durata di conservazione dei cuori dei donatori attraverso miglioramenti al NEHP. I loro precedenti esperimenti hanno dimostrato che un passaggio fondamentale è filtrare il perfusato per rimuovere tutte le molecole più piccole di 26 kilodalton. Senza questo, per ragioni sconosciute, i cuori diventano rapidamente inutilizzabili per i trapianti.
Qui, Bartlett e i suoi colleghi hanno mantenuto in vita i cuori di 30 maiali immaturi e 10 giovani per vari periodi con varianti sperimentali di NEHP. Ad esempio, il perfusato per tutti i cuori dei donatori era una soluzione di plasma sanguigno e globuli rossi concentrati (da altri maiali sani), elettroliti, glucosio e antibiotici. Il perfusato è stato pompato attraverso il cuore ad una velocità media di 0,7 millilitri al minuto per grammo di peso cardiaco e sostituito ogni 60 minuti.
HEHP: con una differenza
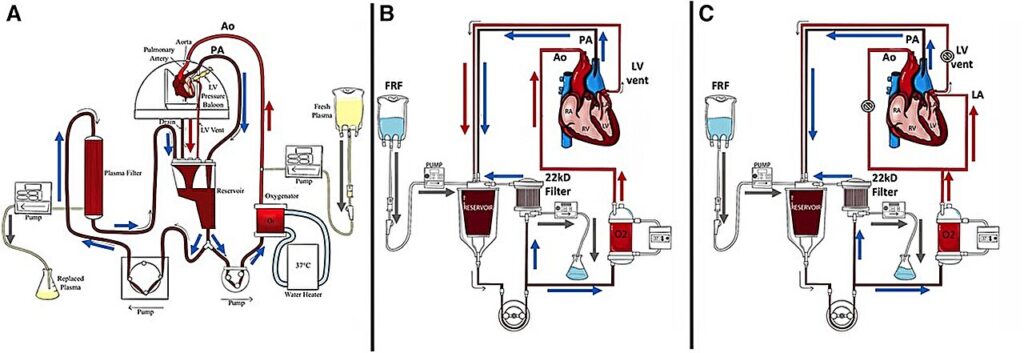
Hanno poi confrontato gli effetti di tre varianti: NEHP con emofiltrazione per purificare continuamente il perfusato e rimuovere le tossine (10 cuori di maiale immaturi); NEHP in cui la componente plasmatica nel perfusato veniva scambiata continuamente (cinque cuori immaturi); e controllare NEHP senza modifiche (15 cuori immaturi).
Per testare questi metodi su cuori più grandi, hanno utilizzato anche il NEPH con emofiltrazione su cinque cuori di suini giovani e il NEPH con un’ulteriore modifica (perfusione atriale sinistra intermittente o iLA) su altri sette cuori di giovani, per monitorare la funzione cardiaca. Nell’iLA, un volume fisso di sangue viene iniettato nell’atrio sinistro a intervalli regolari, per testare la sua continua capacità di espellere questo sangue.
Gli autori hanno monitorato la salute dei cuori preservati in tempo reale controllandone visivamente la contrattilità, il ritmo, il colore e l’edema e misurando la concentrazione di lattato (un sottoprodotto del danno cellulare) ogni ora. Ciascun cuore è stato mantenuto fino a quando non è andato in asistolia o aritmia, ha mostrato una pressione sanguigna sistolica minima nel ventricolo sinistro o ha mostrato concentrazioni elevate di lattato per almeno due ore.
Forti miglioramenti
Tutti i cuori di controllo sono morti tra le 10 e le 24 ore dopo la rimozione dal donatore, mentre tutti i cuori che erano stati mantenuti con modifiche al NEPH standard sono sopravvissuti per tutte le 24 ore. Gli autori concludono che l’emofiltrazione, la plasmaferesi e l’iLA rappresentano miglioramenti importanti che consentono la conservazione di routine dei cuori per oltre un giorno. Non è ancora possibile rispondere a quale degli ultimi tre metodi sia migliore.
“Penso che la differenza maggiore si avrà quando estenderemo i nostri esperimenti oltre le 24 ore, quando forse lo scambio plasmatico è migliore in quanto le tossine più grandi possono essere rimosse. Anche iLA sembra un notevole miglioramento, poiché in linea di principio consentirebbe di utilizzare NEPH su cuori che hanno subito lesioni o hanno una funzione borderline nel donatore”, ha affermato Bartlett.
Più cuori disponibili per il trapianto
“Questo lavoro potrebbe in definitiva aumentare il pool di donatori. In primo luogo, estendendo il tempo di conservazione, superando così le limitazioni dovute alla logistica. In secondo luogo, fornendo una valutazione obiettiva della vitalità di ciascun potenziale donatore di cuore, per ridurre il numero che attualmente non lo è utilizzati quando non è chiaro come funzionano all’interno del donatore,” ha detto il dottor Alvaro Rojas-Pena, ricercatore presso lo stesso istituto e autore corrispondente dello studio.
“La sfida principale per l’applicazione clinica sarà la validazione dei metodi sugli esseri umani. A tal fine, abbiamo iniziato a lavorare con cuori umani rifiutati per il trapianto”, ha affermato Rojas-Pena.

